
Einleitung
Neue Viren, sogenannte emergente Viren, stellen eine Bedrohung für die menschliche Gesundheit dar, deren Ausmaß nicht unterschätzt werden sollte. Diese Viren haben die Fähigkeit erlangt, Menschen zu infizieren, entweder als Folge einer Übertragung zwischen verschiedenen Spezies oder durch natürlich auftretende Veränderungen im viralen Genom¹. Infektionen durch emergente Viren führen häufig zu schweren Erkrankungen oder sogar zum Tod, da das menschliche Immunsystem möglicherweise nicht in der Lage ist, ein unbekanntes Virus zu bekämpfen, insbesondere wenn es zoonotischen Ursprungs ist (siehe Literatur zur weiteren Lektüre²).
Verschiedene Faktoren begünstigen das Auftreten und die Verbreitung emergenter Viren³. Dazu zählen ökologische Faktoren wie die Abholzung von Wäldern zur Gewinnung neuer Flächen für Entwicklungszwecke sowie unser Lebensstil, der durch globale Mobilität und internationalen Handel geprägt ist. Der Verlust von Lebensräumen erhöht somit die Wahrscheinlichkeit, dass Menschen, Haustiere und Nutztiere mit Wildtierarten in Kontakt kommen, die ursprünglich in isolierten Gebieten lebten und daher zuvor nicht als natürliche Wirte emergenter Viren in Erscheinung traten. Darüber hinaus ermöglichen die Rahmenbedingungen einer globalisierten Gesellschaft mit zunehmender Reisetätigkeit auch die weltweite Verbreitung pathogener Viren, noch bevor klinische Symptome auftreten.
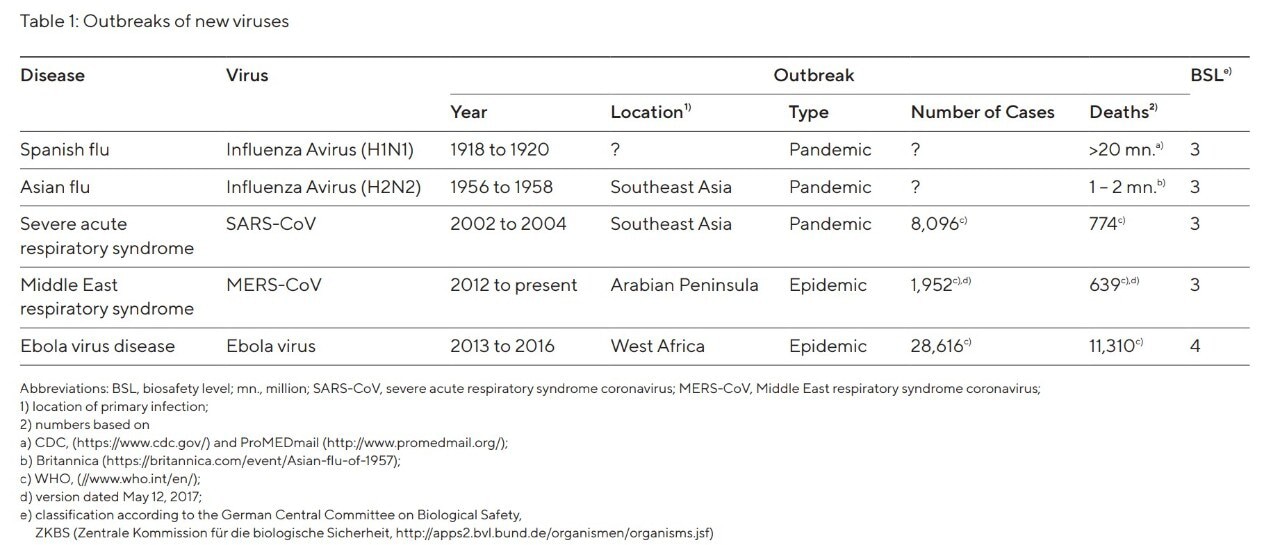
In den letzten 100 Jahren kam es zu mehrfachen Einträgen emergenter Viren in die menschliche Bevölkerung, die zu lokalen Epidemien oder weltweiten Ausbrüchen (Pandemien; siehe Tabelle 1) führten. Insbesondere das Ebola-Virus hat zuletzt weltweit Besorgnis ausgelöst, da die Ebola-Epidemie in Westafrika, die mehr als 11 000 Todesopfer forderte, auf verheerende Weise die von emergenten Viren ausgehende Gefahr verdeutlichte⁴. Die Forschung an emergenten Viren ist häufig auf Hochsicherheitslabore der biologischen Sicherheitsstufen (BSL) 3 und 4 beschränkt (siehe Tabelle 1). Die Arbeit in BSL-4-Laboren ist äußerst arbeitsintensiv, kostenaufwendig und nur an wenigen Standorten erlaubt, sodass rasche wissenschaftliche Fortschritte bei der Charakterisierung viraler Pathogene und der Entwicklung antiviraler Medikamente nur schwer zu erzielen sind.
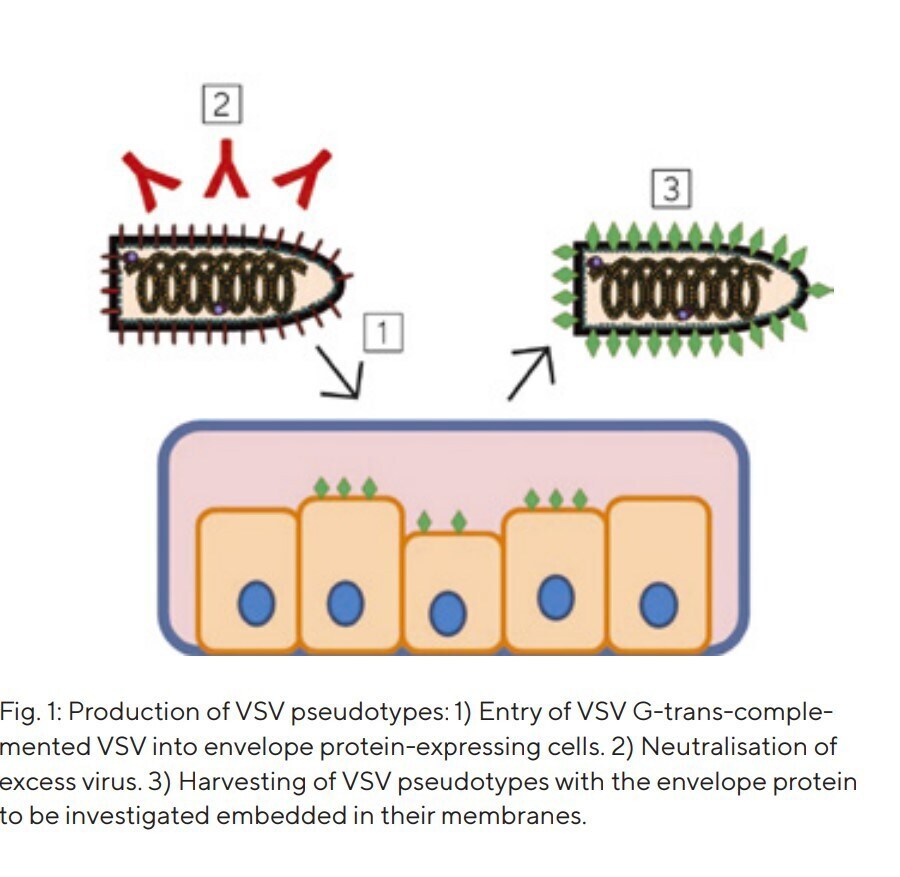
Vor diesem Hintergrund stellen Virus-Pseudotypen eine attraktive Möglichkeit dar, den Eintritt hochpathogener Viren in Zellen sicher und effizient zu untersuchen. Dies ist möglich, da nicht der gesamte Erreger analysiert wird, sondern lediglich jene Komponenten, die den Eintritt in die Wirtszelle vermitteln, nämlich die Hüllproteine. Diese stellen den Schlüssel für den Viruseintritt in Zellen dar. Im Fall von Virus-Pseudotypen werden die Hüllproteine hochpathogener Viren in ein Trägervirus eingebaut (Pseudotypisierung), das sich nicht autonom replizieren kann, d. h. replikationsdefizient ist. Häufig verwendete Systeme zur Pseudotypisierung basieren auf Rhabdoviren (z. B. dem vesikulären Stomatitisvirus, VSV; Abb. 1) und Retroviren.
Ziel dieser Studie war es zu überprüfen, ob der durch Hüllproteine vermittelte Eintritt von Virus-Pseudotypen den Zelleintritt intakter Viren widerspiegelt. Darüber hinaus wurde untersucht, welchen Einfluss der Reinheitsgrad der verwendeten Reagenzien, in diesem Fall des Laborwassers, auf die Herstellung von Virus-Pseudotypen hat.
Materialien und Methoden
HEK-293T-, MDCKII- und Vero-E6-Zellen wurden in Dulbecco’s Modified Eagle Medium (DMEM), ergänzt mit 10 % fötalem Kälberserum (FCS) und 1 % Penicillin/Streptomycin-Lösung, bei 37 °C und 5 % CO₂ inkubiert. Für das Passagieren und Ausplattieren wurden die Zellen mit phosphatgepufferter Salzlösung (PBS) gewaschen und durch Inkubation mit Trypsin | EDTA abgelöst.
Zur Herstellung von VSV-Pseudotypen wurden Plasmide der folgenden viralen Hüllproteine als Expressionsvektoren verwendet: VSV-Glykoprotein (VSV G), Ebola-Virus-Glykoprotein (EBOV GP), Spike-Glykoprotein des Middle East Respiratory Syndrome Coronavirus (MERS-CoV S), Hämagglutinin (HA) und Neuraminidase (NA) des Influenza-A-Virus, das für die Pandemie der „Spanischen Grippe“, H1N1 (1918), verantwortlich war. Zusätzlich wurde ein Expressionsplasmid für Dipeptidylpeptidase 4 (DPP4) eingesetzt. Ein leeres Expressionsplasmid diente als Kontrolle. HEK-293T-Zellen wurden mittels Calcium | Phosphat-Präzipitation transfiziert, wobei alle Puffer und Lösungen entweder mit demineralisiertem Wasser oder mit Sartorius Arium Pro VF Reinstwasser hergestellt wurden.
Herstellung von Reinstwasser
Das verwendete Arium Pro VF Reinstwasser wurde wie von Nitzki und Herbig (2013) beschrieben hergestellt⁵. Dieses Wasser weist einen TOC-Gehalt (Total Organic Carbon, d. h. organisch gebundener Kohlenstoff) von < 2 ppb sowie eine Leitfähigkeit von 0,055 μS/cm (entspricht einer spezifischen Resistivität von 18,2 MΩ × cm) auf, kompensiert auf 25 °C.
Herstellung von VSV-Pseudotypen
Zur Generierung von VSV-Pseudotypen wurde ein replikationsdefizienter VSV-Vektor eingesetzt, bei dem die genomische Information für das VSV-Glykoprotein, VSV G, durch zwei Reportergene ersetzt wurde, nämlich offene Leserahmen (ORFs), die für das grün fluoreszierende Protein (GFP) und die Firefly-Luciferase (fLUC) kodieren. Zur Vermehrung dieses Virus (VSV*ΔG-fLUC) muss VSV G in trans bereitgestellt werden (z. B. durch Transfektion eines Expressionsplasmids). Die VSV-Pseudotypen wurden wie in Hoffmann et al. (2016) beschrieben hergestellt⁶.
Vorbehandlung der Zielzellen mit Sialidase oder Inhibitoren:
MDCKII-Zellen wurden mit 200 mU rekombinanter Sialidase behandelt, um terminale Sialinsäuren von Glykoproteinen und Glykolipiden der Plasmamembran zu entfernen. Um zu prüfen, ob der durch Hüllproteine vermittelte Eintritt von VSV-Pseudotypen in Zellen von einem sauren pH-Wert und der Aktivität zellulärer Cysteinproteasen abhängt, wurden Vero-E6-Zellen mit 50 nM Bafilomycin A1 oder 50 μM E-64d inkubiert. Die eingesetzten Substanzen wurden im Zellkulturmedium verdünnt; die Inkubation erfolgte für 2 Stunden bei 37 °C und 5 % CO₂. Unbehandelte Zellen dienten als Kontrollen.
Analyse des durch Hüllproteine vermittelten Eintritts in die Wirtszelle:
Die Zielzellen wurden für 1 Stunde mit VSV-Pseudotypen inkubiert, anschließend mit PBS gewaschen und für weitere 16–20 Stunden im Zellkulturmedium inkubiert. Danach wurden die Zellen unter Verwendung eines Luciferase-Lysepuffers lysiert, und die Luciferase-Aktivität in den Zelllysaten wurde mit einem Chemiluminometer unter Verwendung kommerziell erhältlicher Testkits gemessen, um die Effizienz der Transduktion (d. h. den Eintritt der Pseudotypen in die Wirtszelle) zu bestimmen.
Ergebnisse
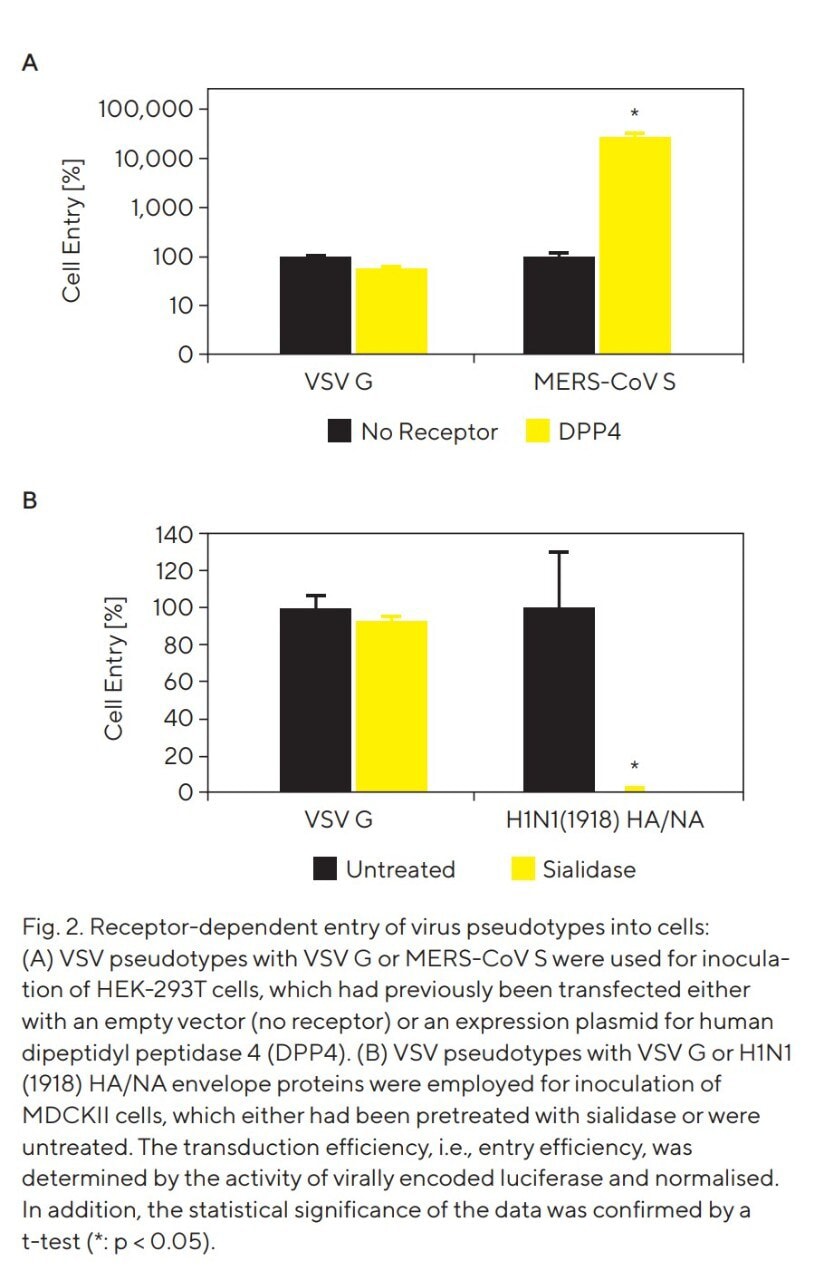
Es ist bekannt, dass das Middle East Respiratory Syndrome Coronavirus (MERS-CoV, früher als humanes Coronavirus, EMC = hCoV-EMC bezeichnet) über die Interaktion zwischen dem viralen Spike-Glykoprotein (S) und dem zellulären Membranprotein Dipeptidylpeptidase 4 (DPP4) an die Zelloberfläche bindet und dadurch den Zelleintritt ermöglicht⁷. Um zu überprüfen, ob dies auch im Kontext von VSV-Pseudotypen zutrifft, wurden Zielzellen mit einem Expressionsvektor für DPP4 oder mit einem leeren Expressionsplasmid (kein Rezeptor) transfiziert. Wie erwartet führte die gezielte Expression von DPP4 zu einer signifikanten Steigerung des Eintritts von VSV-Pseudotypen in die Wirtszellen, sofern diese das MERS-CoV-S-Protein in ihrer Hülle trugen (siehe Abb. 2A).
Influenzaviren vom Typ A, die Erreger der Influenza, benötigen terminale Zuckerstrukturen, sogenannte Sialinsäuren, die als natürliche Modifikationen von Glykoproteinen und Glykolipiden der Zellmembran vorkommen, als Rezeptoren zur Vermittlung des Eintritts in Zielzellen (siehe Literatur zur weiteren Lektüre⁸). Um zu untersuchen, ob die Einlagerung von Influenzavirus-Hüllproteinen in VSV-Pseudotypen ebenfalls zu einem sialinsäureabhängigen Zelleintritt führt, wurden VSV-Pseudotypen mit HA/NA von H1N1 (1918) eingesetzt und die Sialinsäuren enzymatisch von der Oberfläche der Zielzellen entfernt. Wie erwartet führte die Entfernung der Sialinsäuren zu einer drastischen Abnahme des Eintritts von VSV-Pseudotypen in die Wirtszellen, die HA/NA von H1N1 (1918) in ihrer Hülle enthielten (siehe Abb. 2B). Dieser Befund bestätigt, dass Virus-Pseudotypen den Eintrittsmechanismus authentischer Influenzavirus-A-Viren in Zellen widerspiegeln.
Die Aktivierung der Ebola-Virus-Glykoproteine während des Zelleintritts ist pH-abhängig und erfordert die Aktivität von Cysteinproteasen
Das Glykoprotein des Ebola-Virus (EBOV GP) wird posttranslational so modifiziert, dass es multiple Oligosaccharide enthält, und es wird angenommen, dass diese dichte Ansammlung von Glykanen das Virus vor einer effizienten Erkennung durch das menschliche Immunsystem schützt⁹. Während des Eintritts in die Wirtszelle muss jedoch ein Teil der EBOV GP, der den Großteil der Zucker-modifikationen trägt, entfernt werden¹⁰. Dieses funktionelle Priming wird durch zelluläre Cysteinproteasen¹¹ vermittelt, die in endosomalen Vesikeln vorkommen und nur bei niedrigem endosomalem pH aktiv sind.
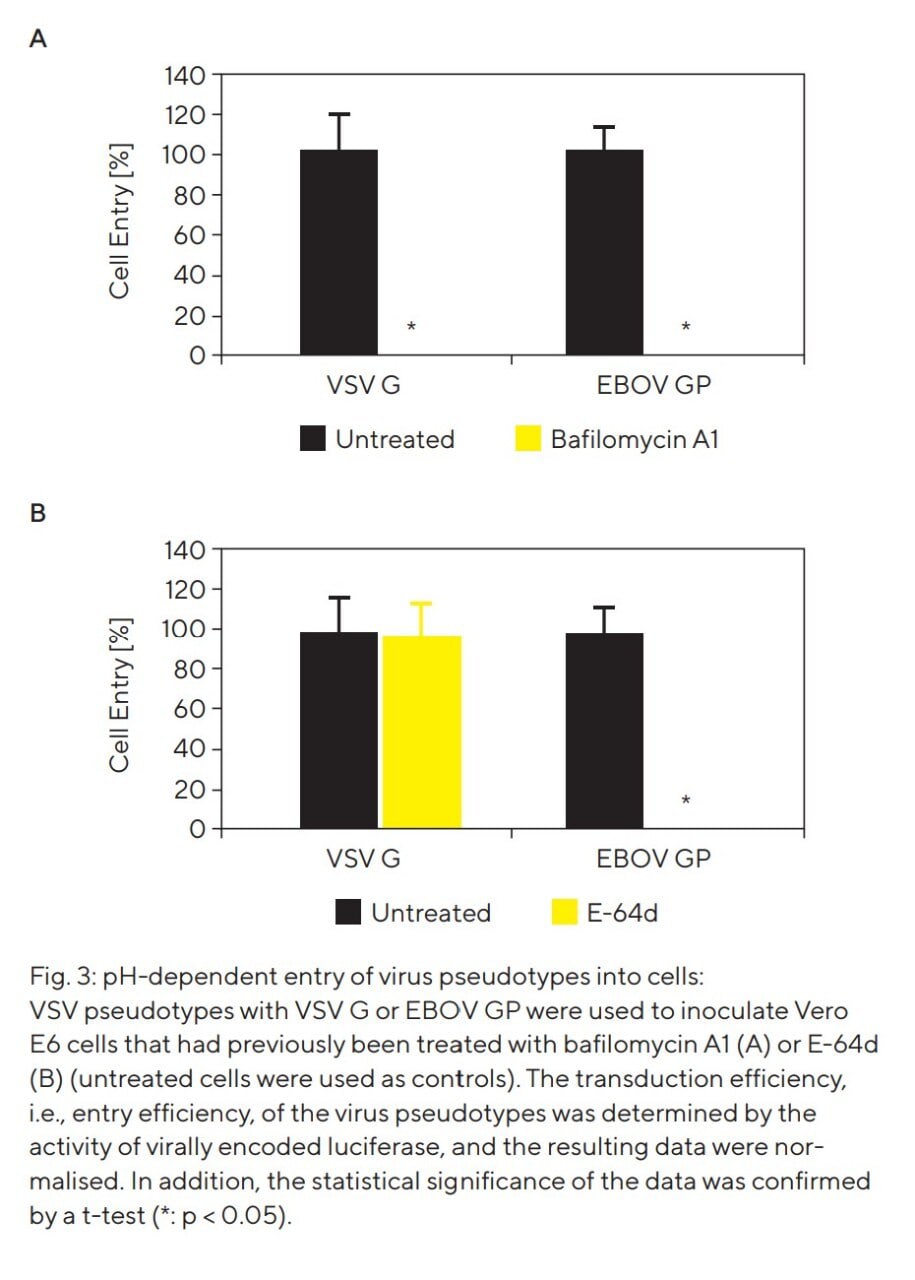
Im Folgenden untersuchten wir, ob der durch EBOV GP vermittelte Eintritt von VSV-Pseudotypen ebenfalls von der Aktivität zellulärer Cysteinproteasen und einem niedrigen pH-Wert abhängt. Zu diesem Zweck wurden VSV-Pseudotypen mit in ihre Hülle eingebautem EBOV GP hergestellt und anschließend zur Inokulation von Zielzellen verwendet, die zuvor mit Bafilomycin A1 (verhindert die Ansäuerung der Endosomen durch Blockade der Protonenpumpe) oder einem Cysteinprotease-Inhibitor (E-64d) inkubiert worden waren. Die Ergebnisse zeigten, dass der durch EBOV GP vermittelte Zelleintritt im Kontext von VSV-Pseudotypen ebenfalls von einer sauren Umgebung (siehe Abb. 3A) und der Aktivität von Cysteinproteasen (siehe Abb. 3B) abhängt. Darüber hinaus konnten wir zeigen, dass die Behandlung mit E-64d spezifisch den durch EBOV GP vermittelten Zelleintritt blockiert, da der durch VSV-G vermittelte Eintritt von Pseudotypen unabhängig von Cysteinproteasen ist, obwohl er von einem niedrigen endosomalen pH abhängt.
Der Reinheitsgrad des verwendeten Laborwassers beeinflusst die Qualität von VSV-Pseudotypen
Nachdem in den vorangegangenen Versuchen gezeigt werden konnte, dass VSV-Pseudotypen geeignete Modelle zur Untersuchung des Zelleintritts hochpathogener Viren in Wirtszellen darstellen, galt es im nächsten Schritt, den spezifischen Einfluss des Reinheitsgrades des verwendeten Laborwassers auf die Qualität der VSV-Pseudotypen zu klären. Während der Herstellung von VSV-Pseudotypen werden verschiedene Puffer und Lösungen eingesetzt, die sämtlich mit Wasser hergestellt werden. Dabei ist jedoch zu beachten, dass nicht jede Art von Wasser für die Herstellung dieser Reagenzien geeignet ist. Vielmehr muss für den Laborgebrauch der richtige Reinheitsgrad gewählt werden.
Um zu untersuchen, ob die Verwendung von Reinstwasser zu VSV-Pseudotypen höherer Qualität führt, wurden in einem parallelen Experiment zwei Chargen von VSV-Pseudotypen erzeugt: Eine Charge wurde unter Verwendung von demineralisiertem Wasser aus einer zentralen Laborwasserversorgung (Leitfähigkeit 3,7–4,1 μS/cm bei 19 °C) als Basislösungsmittel für alle Lösungen und Puffer hergestellt, während eine weitere Charge unter Verwendung von Lösungen und Puffern auf Basis von Arium Pro VF Reinstwasser (Leitfähigkeit 0,055 μS/cm, auf 25 °C kompensiert) erzeugt wurde. Als Hüllproteine wurden EBOV GP und MERS-CoV S untersucht. Nach paralleler Herstellung der VSV-Pseudotypen unter identischen Inkubationsbedingungen wurden die Zielzellen inokuliert und der durch Hüllproteine vermittelte Eintritt der VSV-Pseudotypen quantifiziert.
Dieser Versuchsaufbau zeigte, dass der Zelleintritt (als Parameter für den Qualitätsgrad) der VSV-Pseudotypen, die unter Verwendung von Arium Pro VF Reinstwasser als Basislösungsmittel für alle Puffer und Lösungen hergestellt wurden, signifikant höher war als der der Pseudotypen, bei deren Herstellung demineralisiertes Wasser verwendet wurde (Abb. 4).
Zusammenfassung
Im Rahmen dieser Studie wurden Virus-Pseudotypen auf der Basis eines replikationsdefizienten vesikulären Stomatitisvirus (VSV) hergestellt, und die Hüllproteine verschiedener hochpathogener Viren wurden untersucht. Wir konnten zeigen, dass der Eintritt in die Wirtszelle auf denselben Rezeptormolekülen und biochemischen Prozessen beruht, wie sie für authentische Viren beschrieben sind. Darüber hinaus zeigten wir, dass die Verwendung von Reinstwasser bei der Herstellung von VSV-Pseudotypen zu einer Optimierung dieses Prozesses führte. Zukünftige Untersuchungen sollten darauf ausgerichtet sein, die Grundlage dieser Beobachtung zu klären: Beruht sie auf einer erhöhten Menge produzierter VSV-Pseudotypen, auf einem effizienteren Zelleintritt oder auf einer verbesserten Stabilität der Pseudotypen? So kann beispielsweise spekuliert werden, dass das Fehlen von Salzen, Proteinasen oder Lipasen bei Verwendung von Reinstwasser die Stabilität der VSV-Pseudotypen erhöht.
Zusammenfassend lässt sich festhalten, dass Virus-Pseudotypen wichtige Werkzeuge zur Untersuchung des Zelleintritts hochpathogener Viren darstellen. Da diese Virus-Pseudotypen die Forschung an hochpathogenen Viren nicht auf BSL-3- oder BSL-4-Labore beschränken, wird es einer größeren Anzahl wissenschaftlicher Einrichtungen ermöglicht, entsprechende Forschungsarbeiten durchzuführen.
Infolgedessen kann der Zelleintritt emergenter Viren charakterisiert und geeignete Nachweisverfahren sowie antivirale Strategien (Medikamente, Impfstoffe) schneller entwickelt werden. Der Einsatz von Pseudotypen reduziert zudem den erheblichen Arbeitsaufwand in Hochsicherheitslaboren, die Ganzkörperschutzanzüge erfordern, sowie die hohen Kosten und die mit solchen Laborarbeiten verbundenen Einschränkungen (z. B. kein Zugang zu Geräten, die sich nicht direkt innerhalb des Hochsicherheitslabors befinden). Darüber hinaus minimieren Virus-Pseudotypen im Vergleich zu authentischen hochpathogenen Viren das Infektionsrisiko für das Laborpersonal nach unbeabsichtigter Exposition und stellen damit einen wesentlichen Sicherheitsaspekt dar.
Die Optimierung des Produktionsprozesses, beispielsweise durch den Einsatz hochreiner Reagenzien, insbesondere wasserbasierter Reagenzien, kann zusätzlich dazu beitragen, die Sensitivität nachfolgender Testverfahren zu verbessern, die Produktionsmengen zu erhöhen und damit die Produktionskosten weiter zu senken.
Literatur
1 Li, W. et al. Animal origins of the severe acute respiratory syndrome coronavirus: Insight from ACE2-Sprotein interactions. Journal of Virology 2016; 80: 4211–4219.
2 Mandl, J. et al. Reservoir host immune responses to emerging zoonotic viruses. Cell 2015; 160: 20–35.
3 Morse, S. S. Factors in the emergence of infectious diseases. Emerging Infectious Diseases 1995; 1: 7–15.
4 Shiwani, H. A. et al. An update on the 2014 Ebola outbreak in Western Africa. Asian Pacific Journal of Tropical Medicine 2017; 10: 6–10.
5 Nitzki, F., Herbig, E. In situ Hybridisierung – Die Bedeutung von Reinstwasser für RNA Technologien”, GIT Labor-Fachzeitschrift 57. Jahrgang, 3; 2013 [also available in English: In Situ Hybridization: The Importance of Ultrapure Water for RNA Technologies].
6 Hoffmann, M. et al. The glycoproteins of all filovirus species use the same host factors for entry into bat and human cells but entry efficiency is species dependent. PLoS One; 2016, Vol. 11.
7 Raj, V. S. et al. Dipeptidyl peptidase 4 is a functional receptor for the emerging human coronavirus-EMC. Nature 2013; 495: 251–254.
8 De Graaf, M., Fouchier, R. A. M. Role of receptor binding specificity in influenza A virus transmission and pathogenesis. The EMBO Journal 2014; 33: 781–935.
9 Cook, J. D., Lee, J. E. The secret life of viral entry glycoproteins: Moonlighting in immune evasion. PLoS Pathogens 2013; Vol. 9.
10 White, J. M., Schornberg, K. L. A new player in the puzzle of filovirus entry. Nature Reviews Microbiology 2012; 10: 317–322.
11 Chandran, K. et al. Endosomal proteolysis of the Ebola virus glycoprotein is necessary for infection. Science 2005; 308: 1643–1645.
