EU-GMP-Anhang 1: Sind Sie für die Anforderungen gerüstet?
Was ist EU GMP Anhang 1?
Anhang 1 ist ein rechtsverbindlicher Teil des EU-Leitfadens zur Guten Herstellungspraxis (EU-GMP), der Informationen über die Herstellung steriler Arzneimittel enthält. Die neue Fassung des Anhangs 1 wurde am 25. August 2022 veröffentlicht und wird ein Jahr später, am 25. August 2023, in Kraft treten.
Was deckt Anhang 1 ab?
Anhang 1 enthält umfassende Leitlinien für die Planung, den Bau und die Instandhaltung von Einrichtungen und Ausrüstungen, die bei der Herstellung von Arzneimitteln verwendet werden. Er enthält auch Leitlinien für Produktionsverfahren, Qualitätskontrolle und Dokumentation.
Anhang 1 gilt für alle sterilen Arzneimittel, die in der EU und im Vereinigten Königreich (UK) hergestellt werden, sowie für solche, die anderswo hergestellt und in die EU und das UK exportiert werden. Er gilt für:
- Fertigprodukte
- Wirkstoffe
- Verpackungsmaterialien
- Produkte in jeder Größe und Kombination
- Beliebige Herstellungsverfahren
- Beliebige Herstellungstechnologien
- Beliebigen Herstellungsumfang (wenn das Ziel die Bereitstellung eines sterilen Produkts ist)
- Die Gestaltung und Kontrolle von Einrichtungen, Ausrüstungen, Systemen und Verfahren
Was sind die größten Kontaminationsrisiken bei der aseptischen Verarbeitung?
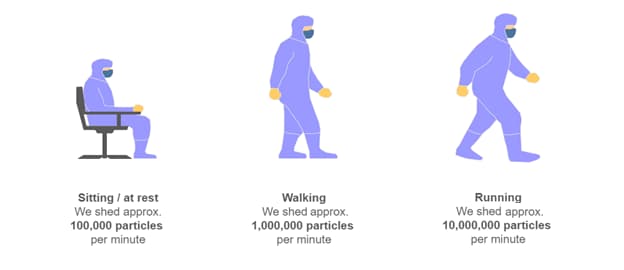
Zu den Kontaminationsquellen in einem Reinraum gehören Rohmaterialien, Verpackungen, Geräte, Flüssigkeiten, Werkzeuge, Prozesse und vor allem Menschen. Mikroorganismen werden von Haaren, Haut, Augen und Schleimhäuten abgesondert.1 Wenn sich Menschen in kontrollierten und sterilen Umgebungen bewegen, sondern sie 10-mal mehr Partikel ab als wenn sie sitzen oder ruhen (Abbildung 1), daher der Grund für klare Richtlinien zum korrekten kontrollierten Verhalten des Personals in Anhang 1 Teil 7.18:
"Aktivitäten in reinen Bereichen, die nicht kritisch für die Produktionsprozesse sind, sollten auf ein Minimum beschränkt werden, insbesondere wenn aseptische Arbeitsgänge durchgeführt werden. Die Bewegung des Personals sollte langsam, kontrolliert und methodisch erfolgen, um eine übermäßige Freisetzung von Partikeln und Organismen durch übermäßige Aktivität zu vermeiden. Das Personal, das aseptische Arbeitsgänge durchführt, sollte sich jederzeit an die aseptische Technik halten, um Änderungen der Luftströmungen zu vermeiden, die Luft minderer Qualität in die kritische Zone einbringen könnten. Die Bewegung in der Nähe der kritischen Zone sollte eingeschränkt und die Behinderung des unidirektionalen Luftstroms (erste Luft) vermieden werden. Eine Überprüfung von Studien zur Visualisierung des Luftstroms sollte als Teil des Schulungsprogramms in Betracht gezogen werden."
Referenzen
1 Brandes, R. Aseptic Processing: Qualifizierung des Personals, Mass & Peither AG-GMP Publishing, April 12, 2012.



